Данный документ является обобщенным мнением специалистов, занимающихся диагностикой, эпидемиологией, клиникой, лечением и профилактикой гепатита С, которые принимали участие в работе научно-практической конференции «Гепатит С (Российский консенсус)» 26-27 сентября 2000 г. в Москве. Это мнение рекомендуется учитывать при подготовке нормативных материалов и в практической работе.
Гепатит С (диагностика, эпидемиология, лечение, профилактика)
В современный период в России имеет место резкая активизация эпидемического процесса гепатита С. Значительный рост показателей заболеваемости острым гепатитом С (3,2 на 100 тысяч населения в 1994 и 19,3 в 1999 году), частое поражение лиц молодого возраста, высокий уровень хронизации с возможным исходом в цирроз и первичный рак печени определяют повышенное внимание к этому заболеванию, актуальность и важность его дальнейшего изучения.
1. Вирус гепатита C.
Вирус гепатита С (ВГС) — член семейства флавивирусов. Геном ВГС представлен однонитевой РНК протяженностью около 10.000 нуклеотидов. ВГС вызывает заболевание только у человека. В экспериментальных условиях воспроизвести инфекцию можно у высших обезьян (шимпанзе и др.). В сыворотке крови больного и вирусоносителя концентрация ВГС, как правило, не превышает 104 в мл., что значительно меньше соответствующих показателей при гепатите В (107 -1010 в мл) и определяет более высокую инфицирующую дозу ВГС по сравнению с вирусом гепатита В (ВГВ). Популяция ВГС крайне неоднородна. Идентифицировано 6 генотипов (классификация по Simmonds), более 90 субтипов и множественных вариантов вируса, обозначаемых как квазивиды. Зарегистрирована территориальная неравномерность циркуляции генотипов ВГС. В Российской Федерации чаще всего выявляют генотипы 1b и 3a этого вируса. Высокая изменчивость ВГС определяет трудности создания вакцины против гепатита С, которой пока нет.
2. Лабораторная диагностика гепатита С.
Лабораторная диагностика гепатита С (ГС) основана на выявлении специфических маркеров инфицирования ВГС (анти-ВГС-IgM/G, РНК ВГС) и должна проводиться диагностическими препаратами отечественных или зарубежных производителей, разрешённых МЗ РФ, строго по инструкции, прилагаемой к набору, в лабораториях, имеющих лицензию на проведение данного вида лабораторных исследований. Алгоритм лабораторного обследования пациентов на наличие ВГС представлен на схеме №1.
Алгоритм обследования пациентов без симптомов поражения печени НА наличие вгс-инфекции
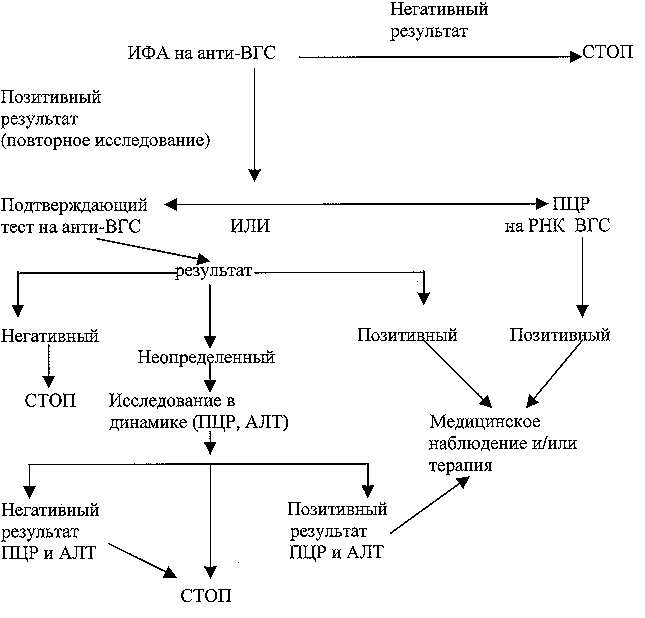
При получении положительного результата в ИФА необходимо использовать дополнительные подтверждающие диагностические препараты отечественного или зарубежного производства и ориентироваться в своем заключении на результаты исследования сывороток в указанных тестах. Результаты проведенных исследований могут трактоваться как: «позитивный», «негативный» и «неопределенный». При «неопределенном» результате через два и более месяцев должно быть проведено дополнительное исследование на наличие маркеров инфицирования ВГС. В качестве подтверждающего метода можно использовать ПЦР с целью выявления РНК ВГС при условии применения диагностических препаратов, одобренных МЗ РФ. Обнаружение РНК ВГС в сыворотках крови с анти-ВГС указывает на текущую инфекцию. Отсутствие РНК ВГС в анти-ВГС позитивных образцах крови не может быть использовано для разграничения прошедшего ГС и «ложнопозитивного» результата лабораторного исследования. Кроме того, у некоторых пациентов регистрируется неустойчивая виремия, что может определять негативный результат выявления РНК ВГС.
Необходимость улучшения качества лабораторных исследований при выявлении маркёров инфицирования ВГС определяет обязательное участие лабораторий в системе мероприятий по осуществлению внешнего контроля качества. Для проведения данной работы необходима научнообоснованная разработка контрольных панелей для тестирования анти-ВГС и РНК ВГС.
3. Эпидемиология гепатита С и профилактические мероприятия.
Источниками заражения ВГС служат больные острыми и хроническими формами ГС-вирусной инфекции, причем основное значение среди них имеют лица с отсутствием желтухи с бессимптомным или малосимптомным течением.
Гепатит С - инфекция с парентеральной передачей возбудителя, проявляющаяся всеми известными формами инфекции — острыми и хроническими с манифестным или бессимптомным течением. Процесс развивается в основном латентно.
В настоящее время большая часть манифестных заболеваний острым ГС является результатом заражения при проведении различных медицинских и немедицинских (в основном внутривенное введение психотропных препаратов) парентеральных манипуляций. Заражение гепатитом С при приеме наркотиков играет ведущую роль и определяет неодинаковую интенсивность эпидемического процесса в разных возрастно-половых группах. Наиболее интенсивно в эпидемический процесс вовлекаются подростки 15-17 лет и молодые взрослые 18-29 лет, преимущественно мужского пола. Среди них формируются специфические группы риска заражения вирусом ГС при многократном использовании контаминированных вируссодержащей кровью игл и шприцев с целью внутривенного введения психотропных препаратов - учащиеся средних (главным образом ПТУ) и высших учебных заведений, мелкие коммерсанты, лица, находящиеся в заключении, безработные и др. Группы риска формируются также из числа лиц, получавших по жизненным показаниям кровь и ее препараты - больные гемофилией, больные, страдающие хронической почечной недостаточностью и получающие сеансы гемодиализа, онкогематологические больные. К группам повышенного риска относятся лица, страдающие различными хроническими заболеваниями (туберкулез и др.) и получающие длительное и многократное стационарное лечение, персонал учреждений службы крови, стационаров (прежде всего сотрудники хирургических, реанимационных отделений, клинико-диагностических лабораторий), имеющие непосредственный контакт с кровью и содержащими кровь секретами, а также доноры, особенно доноры плазмы, подвергающиеся неоднократному неаппаратному плазмаферезу. Эпидемический процесс может проявиться локальными вспышками ГС в случае вовлечения в него значительного числа лиц из групп риска (локальные вспышки в стационарах, центрах плазмафереза и др.).
Естественный компонент эпидемического процесса изучен недостаточно. Материалы эпидемиологического изучения семей больных острым и хроническим ГС подтверждают редкую возможность реализации полового пути передачи возбудителя. Более часто реализация этого пути имеет место среди лиц, ведущих беспорядочную половую жизнь, практикующих секс за деньги, подвергнутых сексуальному насилию, и т.д. Передача ВГС от матерей с острой или хронической формой инфекции — явление редкое, встречается не чаще 5-6 % случаев. Риск заражения указанными естественными путями уступает таковому при гепатите В (ГВ). Профилактические мероприятия в отношении путей и факторов передачи вируса ГС (в т.ч. в очагах хронических форм ВГС-инфекции) проводятся аналогично ГВ. Важное значение имеет медицинское образование населения с акцентами на путях передачи возбудителя ГС и мерах профилактики заражения. Универсальные меры профилактики заражения возбудителями инфекций, передающихся через кровь и половым путем (ГВ, ВИЧ-инфекция, венерические болезни) эффективны и при ГС.
С целью защиты лиц больных хроническим гепатитом С, от возможного заражения ВГА и ВГВ рекомендуется их вакцинация против гепатита А и В.
4. Посттрансфузионный гепатит С и служба крови
Предупреждение пострансфузионного гепатита С — одна из наиболее актуальных задач Службы Крови (СК). Эта задача определяется тремя группами проблем, с которыми сталкивается сегодня СК страны.
4.1. Работа с донорским контингентом
Существенное снижение качества жизни в новой России, ослабление государственной поддержки донорства и работы с населением привели к сокращению числа доноров и к устойчивой тенденции в сторону увеличения доли платных добровольцев, а также к общему увеличению возраста доноров и к практике найма доноров, выдаваемых за родственников. Выходом из этого положения может стать только возобновление эффективной пропагандистской работы СК (чем в СССР занимались, по преимуществу, организации Красного Креста). В настоящее время следует использовать любую возможность (например, в случаях природных катастроф, боевых столкновений и проч.) для демонстрации в средствах массовой информации и телекоммуникации (например, в Интернете) постоянной нехватки донорской крови.
4.2. Лабораторная диагностика
Детекция маркеров гепатита С — одно из слабых мест лабораторной идентификации актуальных в СК вирусов. С одной стороны, отсутствие на рынке надежных систем прямого определения вирусных белков приводит к тому, что до сих пор результаты ИФА-тестирования на антитела к вирусу гепатита С (ВГС) остаются основой выбраковки потенциально опасной по ВГС-инфекции донорской крови в СК. С другой стороны, внедрение рутинной NAT-диагностики (т.е. методов тестирования на нуклеиновые кислоты, в т.ч. ПЦР) российской СК сейчас не под силу. Серьезными потерями оборачивается для СК и отсутствие централизованной компьютерной базы данных по донорам, создание которой является неотложной задачей.
Представляется целесообразным скорейшее поэтапное внедрение методов ПЦР в практику СК. Финансовую поддержку этой работе может обеспечить производство препаратов крови. Кроме того, именно на производстве оказывается возможным экономически более выгодный, нежели индивидуальный, ПЦР-анализ пулированного сырья. Создание и работа ПЦР-лабораторий должны быть обеспечены независимым контролем, а их сотрудники обязаны пройти квалификационную подготовку и независимую оценку. В СК абсолютно необходима также организация централизованных компьютерных баз данных.
4.3. Производство вирусобезопасных препаратов крови
Производство препаратов крови предполагает сегодня два эшелона противовирусной защиты: входной контроль и инактивацию на этапах фракционирования. Входной контроль соответствует той работе, которая проводится на станциях и отделениях переливания крови (п.4.2); инактивация осуществляется прогреванием полупродуктов и обработкой их детергентами и низкими рН; используется также нанофильтрация - для снижения концентрации возможного вируса перед инактивацией. Выходной контроль сегодня не регламентируется, поскольку его надежность ограничена полуколичественным характером ИФА и ПЦР и отсутствием адекватных и недорогих лабораторных систем прямого вирусологического исследования. Представляется целесообразным экспериментальное использование методов NAT для оценки их возможностей в организации выходного контроля производства препаратов крови.
5. Естественное течение гепатита С.
Инфицирование ВГС приводит к развитию острого гепатита С (ОГС), протекающего в манифестной (желтушной) или чаще в латентной (безжелтушной) форме, развивающихся в соотношении не менее чем 1 : 6. Около 17-25% больных ОГС выздоравливают спонтанно, у остальных 75-83% развивается хронический гепатит С. Большинство больных с биохимическими признаками хронического гепатита имеют слабовыраженную или умеренную степень некрозо-воспалительного поражения печени и минимально выраженный фиброз. Отдаленный исход у них неизвестен. Примерно у 26-35% больных хроническим гепатитом С в течение 10-40 лет развивается фиброз печени и может наступить смерть от цирроза печени и его осложнений. У 30-40% больных с циррозом печени возможно формирование рака печени. Спектр клинических исходов при гепатите С представлен на схеме № 2.
Схема № 2 Спектр клинических исходов при гепатите С
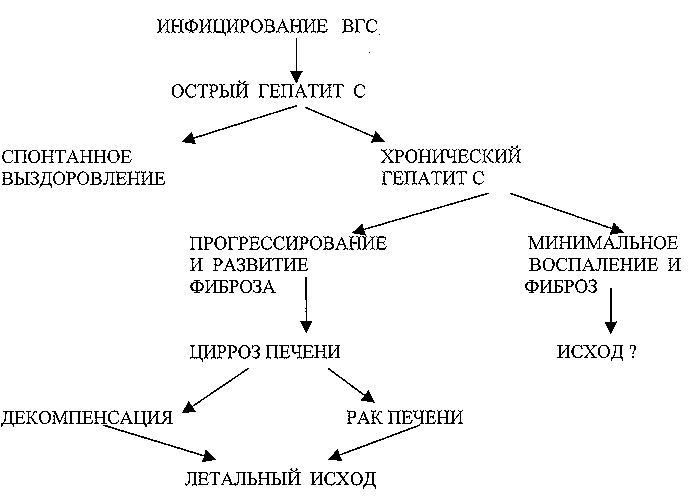
Результатом ГС-инфекции может явиться широкий спектр болезни печени, включая цирроз, рак печени и субклиническое, непрогрессирующее течение хронического гепатита. Сегодня о спонтанном выздоровлении от гепатита С можно говорить в случаях, когда пациент, не получая специфической терапии, хорошо себя чувствует, что сопровождается нормальными биохимическими показателями крови, отсутствием увеличения размеров селезенки и печени и отсутствием в крови РНК ВГС не менее 2 лет после острого гепатита С. Однако окончательные критерии выздоровления пока еще не установлены.
6. Острый гепатит С.
Острый гепатит С — инфекция, вызванная ВГС; в клинически выраженных случаях характеризуется симптомами острого поражения печени, которое чаще всего протекает с умеренной интоксикацией и в большинстве случаев заканчивается развитием хронического гепатита.
6.1. Клиническая диагностика
Диагноз ОГС основывается на комплексе клинических (увеличение печени и селезенки), биохимических (повышение уровня активности аминотрансфераз — АСТ, АЛТ), вирусологических (наличие в крови РНК ВГС и/или анти-ВГС) данных, которые имеют четкую связь с парентеральными манипуляциями за 1-4 месяца до его развития: переливанием крови, хирургическими операциями, первой инъекцией наркотических средств и т.п. Антитела к белкам, кодируемым зоной РНК ВГС NS3 и NS5, не являются абсолютными маркерами как острого, так и хронического гепатита С.
У большинства пациентов отсутствуют признаки острого гепатита. Обнаружение РНК ВГС на фоне анти-ВГС не позволяет отличить острый гепатит С от обострения хронического гепатита С. Диагностика острого гепатита С в большинстве таких случаев должна базироваться на наличии соответствующих данных эпиданамнеза за 1-4 месяца до впервые выявленных признаков гепатита С — анти-ВГС и ферментемии.
После ОГС больной подлежит диспансерному наблюдению в кабинете инфекционных заболеваний территориальной поликлиники.
6.2. Лечение
6.2.1. Интерферонотерапия
В настоящее время интерферонотерапия (ИФН-терапия) занимает лидирующее место в лечении как острого, так и хронического гепатита С. В случаях диагностики острого гепатита С можно рекомендовать лечение альфа-интерферонами сразу после установления диагноза в дозе 3 млн МЕ трижды в неделю в течение 6 месяцев.
6.2.1.1. Мониторинг безопасности ИФН-терапии включает:
Всем больным во время ИФН-терапии обязательно проводят исследование активности АЛТ и клинический анализ крови 1 раз в 2 недели в первый месяц лечения и ежемесячно в дальнейшем. Кроме того, до начала лечения необходимо исследовать показатели функции щитовидной железы и аутомаркеры
-при нормальных уровнях вышеперечисленных показателей необходимо проводить их тестирование - 1 раз в 6 месяцев;
-при измененных уровнях необходим ежемесячный контроль всех показателей.
6.2.1.2. Мониторинг эффективности ИФН-терапии включает:
Исследование АЛТ, РНК ВГС сразу после окончания 6 мес. терапии и в дальнейшем 1 раз в полгода в течение 2-х лет (в случаях стойкого положительного эффекта).
7. Хронический гепатит С.
Хронический гепатит С (ХГС) — это диффузное заболевание печени продол-жительностью 6 и более месяцев, причиной которого является вирус гепатита С.
7.1. Клиническая диагностика
Критериями для постановки диагноза являются увеличение печени и селезенки, гиперферментемия и анти-ВГС в крови сроком не менее 6 месяцев, при исключении других хронических заболеваний печени, согласно международной классификации 1994 года. Точный характер поражения печени, а именно, степень некрозо-воспалительных изменений и стадию фиброза, позволяет определить биопсия печени. Результаты исследования биопсии печени дают точку отсчета у конкретного больного.
Наличие или отсутствие РНК ВГС, как правило, не является диагностическим критерием хронического гепатита С и определяет фазу процесса (активный, неактивный).
7.2. Лечение
Лечение больных с хроническим гепатитом С должно проводиться в центрах, обеспечивающих соблюдение правил санэпидрежима, специалистами-гепатологами (инфекционистами и гастроэнтерологами).
При наличии у больных тяжелых сопутствующих заболеваний пациентам должно проводиться лечение ХГС гепатологами совместно со специалистами согласно профилю заболевания пациента (урологом, онкологом, кардиологом, эндокринологом, венерологом и др.). В большинстве случаев лечение ХГС может осуществляться в амбулаторно-поликлинических условиях.
7.2.1. ИФН-терапия
ИФН-терапия безусловно показана:
-взрослым больным от 18 до 60 лет,
-при постоянном повышении уровней АЛТ,
-при наличии РНК ВГС в крови,
-при наличии в биоптате печени умеренно выраженного воспалительного процесса или фиброза.
В случае наличия вышеперечисленных показаний к ИФН-терапии, первостепенной задачей клинициста является оценка возможной эффективности для конкретного пациента. Основанием для назначения монотерапии ИФН может служить наличие следующих факторов, указывающих с большой долей вероятности на конечный благоприятный лечебный эффект: молодой возраст на момент заражения (до 40 лет), женский пол, отсутствие избыточного веса, повышенного уровня железа и гамма-ГТП в сыворотке крови, повышенные уровни АЛТ, наличие умеренной степени активности процесса и минимального фиброза по данным биопсии печени, невысокий уровень РНК ВГС и «не 1» генотип ВГС. Отсутствие этих факторов может рассматриваться как показание к назначению комбинированной терапии. Стандартной монотерапией альфа-ИФН является введение 3 млн. МЕ препарата трижды в неделю в течение 12 месяцев, при условии исчезновения РНК ВГС через 3 мес. от начала лечения. В случаях обнаружения РНК ВГС после 3 мес. лечения продолжать терапию по указанной схеме нецелесообразно.
При отсутствии показаний к ИФН-терапии необходимо проведение динамического наблюдения и базисного, в основном симптоматического, лечения (особенно при сопутствующих заболеваниях). Контрольные исследования биохимических показателей крови целесообразно исследовать 1 раз в 3 мес.: РНК ВГС, белковый спектр крови, протромбин и альбумин — 1 раз в 6 мес.; УЗИ и альфа-фетопротеин — 1 раз в 12 мес. В случаях проведения только базисной терапии при динамическом обследовании рекомендуется провести повторную биопсию печени через 4-5 лет. Противопоказания к назначению ИФН-терапии представлены в инструкции по применению коммерческих препаратов ИФН.
7.2.1.1. Оценка (мониторинг) эффективности ИФН-терапии при ХГС.
Включает в себя следующие показатели: уровень АСТ или АЛТ, наличие или отсутствие РНК ВГС, временной фактор.
Биохимическая ремиссия в конце лечения — нормализация уровней АСТ и АЛТ сразу после окончания терапии;
Полная ремиссия в конце лечения — нормализация уровней АСТ и АЛТ и исчезновение РНК ВГС из крови сразу после окончания терапии;
Стабильная биохимическая ремиссия — сохранение нормального уровня АСТ и АЛТ через 6 мес. и более после прекращения терапии;
Стабильная полная ремиссия — сохранение нормального уровня АСТ и АЛТ, а также отсутствие РНК ВГС через 6 мес. и более после прекращения терапии;
В случаях достижения стабильной полной ремиссии через 6 мес. после окончания лечения рекомендуется продолжить наблюдение за больным не менее 2-х лет с периодичностью 1 раз в полгода и последующей биопсией печени.
Рецидив болезни — повышение уровня АСТ и АЛТ и / или появление РНК ВГС в крови после прекращения лечения.
Отсутствие лечебного эффекта — отсутствие нормализации уровня АСТ или АЛТ и/или сохранение РНК ВГС в крови в течение 3 мес. после начала лечения и/или в конце лечения.
Любой достигнутый эффект на монотерапию ИФН должен быть учтен клиницистом, т.к. имеет значение для дальнейшей тактики лечения. Мониторинг безопасности терапии при ХГС проводится аналогично острому ГС.
7.2.2. Комбинированная терапия
Рекомендованной к применению комбинированной терапией является сочетание альфа-интерферона с рибавирином для следующих категорий больных ХГС:
- пациентов, у которых выявлены неблагоприятные прогностические факторы, указывающие на низкий уровень эффективности монотерапии ИФН и которые не лечились ранее препаратами интерферона;
— пациентов, у которых произошел рецидив болезни после прекращения лечения интерферонами. Мониторинг эффективности и безопасности комбинированной терапии аналогичен таковому при проведении монотерапии ИФН и дополнительно включает в себя тестовый контроль на беременность с целью ее исключения в течение всего периода лечения и 4-6 мес. после его окончания.
Эффективность комбинированной терапии у больных, которые не отвечали на монотерапию интерфероном, в настоящее время находится в стадии изучения. Пациенты могут участвовать в исследовании различных схем лечения в рамках Протокола клинических испытаний.
7.3. Лечение урсодезоксихолиевой кислотой (УДХК)
Использование УДХК в лечении ХГС является вспомогательным средством. Основным показанием для назначения УДХК следует считать наличие холестаза. Сочетание с интерферонами не увеличивает эффективность альфа-интерферонов в отношении элиминации ВГС, но может уменьшить частоту биохимического рецидива заболевания.
7.4. Лечение хронического гепатита С у больных с аутоиммунными нарушениями
Терапия противовирусными препаратами в настоящее время находится в стадии накопления клинического опыта. Лечение, особенно препаратами интерферона, следует назначать строго индивидуально, желательно в рамках Протокола клинических испытаний, обеспечивающего безопасность терапии. При выраженной клинической и лабораторной картине аутоиммунного заболевания, особенно аутоиммунного гепатита, предпочтение в начале лечения следует отдать преднизолонотерапии.
7.5. Лечение хронического гепатита С у детей
Программа лечения детей с ХГС должна включать в себя только те препараты, безопасность и эффективность которых не вызывает сомнения. Ввиду вялотекущего течения хронического гепатита С и того, что эффективность применения интерферонов у детей находится в стадии изучения, ИФН-терапию детям целесообразно назначать в рамках Протокола клинических испытаний.
7.6. Варианты лечения хронического гепатита С в стадии выраженного фиброза или компенсированного цирроза печени (класс А по Чайльд-Пью)
Лечение подобного контингента больных остается проблематичным из-за небольшой эффективности современных терапевтических средств и плохой их переносимости. Предпочтительным является назначение комбинации альфа-интерферона с рибавирином в рамках Протокола клинических испытаний. При отсутствии эффекта или наличии противопоказаний к рибавирину может применяться длительная монотерапия ИФН с целью получения и сохранения биохимического ответа. Такая стратегия может замедлять прогрессирование болезни, угнетая фиброгенез, и снизить риск развития рака печени. Обязательным является мониторинг исследований, включающий помимо ежемесячного контроля биохимических и клинических показателей крови определение концентрации протромбина, ∂-фетопротеина и УЗИ каждые 6 месяцев.
7.7. Интерферонотерапия больных хроническим гепатитом С с сопутствующими заболеваниями
За последние годы выработаны четкие критерии обоснования назначения интерферонотерапии при хроническом гепатите С. Это в первую очередь профилактика развития цирроза печени (ЦП) и гепатоцеллюлярной карциномы (ГЦК), как исходов хронического гепатита. У пациентов без сопутствующей патологии схемы применения ИФН отработаны и подход к лечению унифицирован. Лечение больных с сопутствующей патологией требует особого подхода, т.е. выработки специальной тактики интерферонотерапии. Этот очень важный принцип индивидуализации лечения помогает просчитать соотношение целесообразность/безопасность и избежать необоснованной терапии и ее осложнений у больного с хроническим гепатитом С и сопутствующим заболеванием. В связи с этим важно убедиться в том, что терапия интерфероном действительно обоснована у данного конкретного пациента (наличие репликации ВГС, наличие стойкого или волнообразного повышения активности АЛТ, в сочетании с умеренной или выраженной активностью гепатита по данным морфологического исследования печени).
При определении показаний к лечению интерфероном у пациента с гепатитом С и сопутствующими заболеваниями очень важно оценить, какая патология является ведущей. Решающим фактором может служить темп прогрессирования сопутствующего заболевания. При наличии сопутствующего заболевания с быстрой прогрессией от терапии интерфероном гепатита С в большинстве случаев следует воздержаться из-за риска осложнений интерферонотерапии, которые могут в свою очередь увеличить темп прогрессии сопутствующего заболевания.
7.7.1. Терапия интерфероном хронического гепатита С у ВИЧ - инфицированных пациентов
Обоснованием назначения интерферона у данной группы пациентов является наличие активного гепатита С (повышение активности трансаминаз, РНК ВГС в сыворотке, морфологические данные, свидетельствующие об активном хроническом гепатите).
Лечение интерфероном у этой категории больных можно проводить в рамках клинических испытаний при отсутствии симптомов ВИЧ-инфекции и выраженной иммуносупрессии (содержание CD4+ клеток более 500/мкл). При этом должны использоваться стандартные дозы препаратов. При условии тщательного мониторинга за уровнем CD4+ клеток и РНК ВИЧ возможно проведение комбинированного лечения: ИФН + рибавирин.
Перспективными являются исследования по безопасности и эффективности проведения антиретровирусной терапии в сочетании с терапией интерфероном у ВГС-ВИЧ коинфицированных пациентов. Их целью является разработка четких показаний к такой терапии, основанных на комплексе показателей: результатов пункционной биопсии печени, иммунного статуса, стадии ВИЧ-инфекции с учетом уровня вирусной нагрузки и генотипа ВГС.
7.7.2. Лечение хронического гепатита С у больных туберкулезом
Эффективность и безопасность лечения интерфероном хронического гепатита С у больных туберкулезом не изучена. Кандидатами на проведение интерферонотерапии по поводу хронического гепатита С в рамках клинических испытаний с использованием стандартных доз ИФН могут являться больные туберкулезом в стадии ремиссии, имеющие клинико-лабораторные и морфологические признаки активно текущего гепатита С.
7.7.3. Лечение хронического гепатита С у больных алкоголизмом и наркоманией
Условием назначения интерферонотерапии гепатита С может быть только полный отказ от употребления алкоголя. Терапия интерфероном лиц, продолжающих употреблять наркотики внутривенно, нецелесообразна из-за высокого риска реинфицирования и осложнений интерферонотерапии на фоне наркотизации. Условием назначения интерферона лицам, употреблявшим наркотики, может быть только полный отказ от приёма наркотиков и наличие 2-х месячного периода ремиссии от последнего употребления наркотика, отсутствие психической и физической зависимости, требующей лекарственной терапии, отсутствие депрессии. Лечение указанных категорий пациентов должно проводиться с использованием стандартных доз ИФН.
7.7.4. Лечение хронического гепатита С у пациентов с патологией почек
Принципиально отличаются подходы к назначению ИФН-терапии у больных с хронической почечной недостаточностью (ХПН), находящихся на программном гемодиализе, в зависимости от планируемой трансплантации почки. У больных, которым не планируется пересадка почки, лечение ИФН назначается при наличии морфологически выраженных изменений в ткани печени, т.к. активность АЛТ не отражает в большинстве случаев активность ХГС. Пункционная биопсия печени у них проводится с учетом общепринятых противопоказаний. Пациентам с ХГС, которые находятся в ходе подготовки к пересадке почки, можно назначать ИФН без учета данных морфологического исследования печени, в стандартной дозе, после каждого сеанса гемодиализа, в рамках Протокола клинических испытаний. Применение рибавирина у этой категории больных противопоказано в связи с риском накопления метаболитов рибавирина в эритроцитах. Больным, подвергшимся аллотрансплантации почек, назначать ИФН для лечения хронического гепатита С не рекомендуется, т.к. это может повысить риск отторжения трансплантата. У этой категории больных перспективным представляется изучение эффективности монотерапии рибавирином.
7.7.5. Лечение интерфероном хронического гепатита С у больных сахарным диабетом
Эффективность и безопасность применения препаратов ИФН для лечения гепатита С у больных сахарным диабетом, получающих инсулин, не изучена. У больных диабетом лечение интерфероном следует проводить с использованием стандартных доз в рамках клинических исследований. Противопоказанием к лечению интерфероном является декомпенсированный сахарный диабет.
7.7.6. Лечение интерфероном больных хроническим гепатитом С и гемофилией
Больным с тяжелой формой гемофилии проведение интерферонотерапии не рекомендуется (в связи с высоким риском образования гематом в местах инъекций). При гемофилии легкой и средней тяжести и наличии клинико-лабораторных показателей активности гепатита С в рамках клинических исследований возможно проведение ИФН-терапии с использованием стандартных доз препарата. Перспективным является изучение эффективности комбинации ИФН + рибавирин. Пункционная биопсия печени пациентам с гемофилией не проводится.
7.7.7. Лечение интерфероном больных хроническим гепатитом С с онкологическими заболеваниями
Лечение хронического гепатита С у пациентов с онкологическими заболеваниями может проводиться с использованием стандартных доз ИФН в рамках клинических исследований при соблюдении следующих условий: клинико-лабораторные и морфологические показатели активности гепатита С, ремиссия по основному заболеванию, отсутствие лучевой терапии или химиотерапии.
7.8. Беременность и гепатит С
Вопросы перинатальной (вертикальной) передачи ВГС-вирусной инфекции (от матери к плоду во время беременности) остаются пока не до конца изученными. Заражение ребенка возможно, если у матери имеется во время беременности и родов активная вирусная репликация. При этом в крови женщины обязательно обнаруживают РНК ВГС. Но даже в этих случаях вертикальный механизм передачи реализуется лишь в 4-10% случаях, т.е. большинство новорожденных не инфицируется во время беременности и родов.
Горизонтальная передача ГC-вируса возможна при тесных контактах матери и ребенка, особенно в первые месяцы жизни, и связана с микротравматизацией слизистых и кожных покровов. При отсутствии повреждения молочной железы (трещин) у родильниц ребенок может находиться на грудном вскармливании. Выявление анти-ВГС у беременной женщины не является показанием к искусственному прерыванию беременности или родоразрешению с помощью кесарева сечения. Лечение гепатита С во время беременности этиотропными препаратами не проводится. При сроках обследования детей, родившихся от матерей с анти-ВГС, необходимо учитывать, что материнские анти-ВГС могут циркулировать в крови ребенка до 1,5 лет. Вследствие этого, не рекомендуется проводить раннее (до 1 года жизни) или частое обследование детей на анти-ВГС, т.е. выявление их до 1-1,5 лет может способствовать ложной диагностике гепатита С у ребенка. У большинства детей, рожденных от матерей с анти-ВГС, к 1,5 годам анти-ВГС исчезают.
Спектр «открытых вопросов», требующих изучения.
Главным, всё ещё не решенным, остаётся вопрос о создании вакцины против гепатита С и следующие вопросы:
I. Клиника
1. Что является критерием полного выздоровления при остром гепатите С?
2. Какие факторы способствуют прогрессирующему и непрогрессирующему естественному течению процесса при ВГС-инфекции?
3. Возможно ли полное выздоровление после проведенной специфической терапии?
4. Каковы морфологические изменения у лиц со стабильной клинико-биохимической и вирусологической ремиссией - спонтанной и после лечения?
II. Диагностика
5. Каково значение антител к белкам, кодируемым различными зонами РНК ВГС при различных формах ВГС-инфекции?
6. Имеются ли и каковы они - новые диагностические признаки ОГС и ХГС в отсутствие желтухи ?
III. Эпидемиология
7. Причины территориальной неравномерности распространения гепатита С ?
8. Какова активность естественных путей передачи ВГС ?
IV. Служба Крови
9. Каков остаточный риск инфицирования реципиентов компонентами крови доноров?
V. Лечение
10. Несмотря на то, что индукторы интерферона и непарентеральная форма интерферона рекомендованы МЗ РФ к применению у больных ОГС и ХГС, участники конференции считают необходимым продолжение изучения эффективности этих препаратов в контролированных исследованиях.
11. Необходимо усовершенствовать и внедрить «унифицированные» карты мониторинга исследования» больных острым и хроническим гепатитом С, получающих лечение противовирусными препаратами.
| Можно рекомендовать в настоящее время | Необходимо изучать | |
| Острый гепатит С | Острый гепатит С | |
| 3 млн МЕ альфа-ИФН трижды в неделю в течение 6 мес. | Оптимальная схема и длительность ИФН-терапии (ежедневное введение, более 6 мес.). | |
| Хронический гепатит С | Хронический гепатит С | |
| Стандартная монотерапия альфа-интерферфероном - 3 млн МЕ трижды в неделю у больных с благоприятными для эффективности прогностическими признаками в течение 12 мес., если РНК ВГС перестаёт обнаруживаться через 3 мес. от начала лечения. | Исследование новых схем монотерапии ИФН (ежедневное введение, повышение дозы). | |
| Комбинированная терапия а-ИФН-3 млн МЕ трижды в неделю с ребетолом 1000-1200 мг Ежедневно для следующих категорий больных: 1. Не получавших ранее ИФН-терапии. 2. С рецидивом после отмены ИФН-терапии. | Исследование эффективности комбинированной терапии у категории «неответивших» на ИФН-терапию. | |
| Изучение эффективности парентеральных форм а-ИФН у детей. | ||
| Изучение эффективности и безопасности новых препаратов, не утвержденных для лечения ГС (иммуномодуляторов, противовирусных, биодобавок и т.п.). | ||
| Изучение эффективности комбини-рованной терапии а-ИФН с ремантадином. | ||
| Изучение эффективности и безопасности этиотропной терапии ХГС у лиц: -с аутоиммунными нарушениями; -с тяжелыми сопутствующими заболеваниями; -с микст-гепатитами (B и D); -у ВИЧ-инфицированных. | ||
| Цирроз печени | Цирроз печени | |
| Длительная монотерапия ИФН при условии сохранения положительного биохимического ответа во время лечения. | Изучение эффективности комбинированной терапии а-ИФН с рибавирином. | |
| УДХК в случаях развития холестаза. |


